Chemiker der Marburger Uni beschreiben Aminosäure-Imitat
 Marburg 14.10.2010 (wm/red) Marburger Chemiker haben ein Aminosäure-Imitat hergestellt, das sich in Proteine einbauen lässt, die dadurch ihre Beweglichkeit einbüßen. Die neue Verbindung soll es leichter machen, künstliche Proteine zu synthetisieren, deren räumliche Gestalt sich präzise vorhersagen lässt. Das US-amerikanische Wissenschaftsmagazin „Proceedings of the National Academy of Sciences“ berichtet in der aktuellen Ausgabe über die Ergebnisse des Forscherteams um Professor Lars-Oliver Essen und Professor Armin Geyer von der Philipps-Universität.
Marburg 14.10.2010 (wm/red) Marburger Chemiker haben ein Aminosäure-Imitat hergestellt, das sich in Proteine einbauen lässt, die dadurch ihre Beweglichkeit einbüßen. Die neue Verbindung soll es leichter machen, künstliche Proteine zu synthetisieren, deren räumliche Gestalt sich präzise vorhersagen lässt. Das US-amerikanische Wissenschaftsmagazin „Proceedings of the National Academy of Sciences“ berichtet in der aktuellen Ausgabe über die Ergebnisse des Forscherteams um Professor Lars-Oliver Essen und Professor Armin Geyer von der Philipps-Universität.
Starrer Riegel hält Proteine in Form
Proteine bestehen aus Ketten von Aminosäuren. In der Natur finden 20 Aminosäure-Typen Verwendung. Neue, künstlich hergestellte Formen könnten zu Proteinen mit erwünschten Eigenschaften führen. „Weltweit suchen Chemiker und Biochemiker nach neuen Aminosäuren, die sich in Proteine integrieren lassen“, erklärt Armin Geyer. Er und seine Kollegen sind auf dem Weg einen großen Schritt weitergekommen. Die von ihnen beschriebene Verbindung geht Wechselwirkungen mit benachbarten Strukturen innerhalb des Proteins ein, in das sie eingebaut wird. Dadurch wird dessen dreidimensionale Form bestimmt.
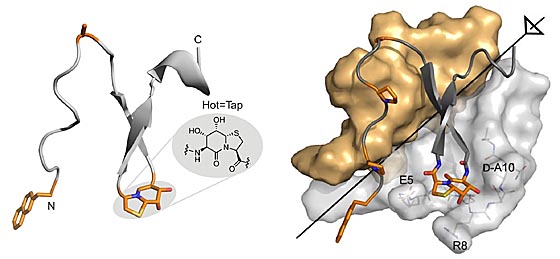
Die Wissenschaftler wählten ein synthetisches Minimal-Protein aus. Sie ersetzten zwei seiner herkömmlichen Aminosäuren durch ein Imitat mit dem Namen „Hot=Tap“, das die Gestalt einer Haarnadelkurve hat. Hot=Tap hält die benachbarten Aminosäureketten wie ein Scharnier in einer vorhersagbaren Form fest. Als stabile Oberflächenstrukturen können sie ganz bestimmte Antikörper binden, vergleichbar einem Schlüssel, der nur in das entsprechende Schloss passt.
Während ein Protein normalerweise seine Gestalt in Grenzen ändern kann wie ein Gummiball, sorgt Hot-Tap für eine feste Form. Dies ist Voraussetzung für spezifische Interaktionen, wie sie von Präparaten erwartet wird, die keine unerwünschten Nebenwirkungen hervorrufen. „Für planbare Architekturen von Aminosäureketten besteht großer Bedarf in der medizinischen Forschung“, erläutert Lars-Oliver Essen. Die Wissenschaftler haben sich als ein erstes Anwendungsbeispiel die Alzheimer-Krankheit vorgenommen.
Originalveröffentlichung
Björn Eckhardt & al.: Structural characterization of a β–turn mimic within a protein-protein interface, PNAS, Vorab-Onlinepublikation 11. Oktober 2010










