13.08.2023 (wm/red) Wie Bakterien CO2 aus der Atmosphäre in Bio-Kraftstoffe verwandeln können, wird am SYNMIKRO-Forschungszentrum und dem Chemie-Department der Universität Marburg erforscht. Für seine Forschung zur biologischen Kohlendioxidfixierung von Mikroorganismen erhält Dr. Jan Schuller den Forschungspreis 2023 der Vereinigung für Allgemeine und Angewandte Mikrobiologie (VAAM). Der Mikrobiologe untersucht Bakterien und ihre Enzymausstattung. Er klärte auf, wie enzymatische „Nano-Drähte“ eine überraschend effiziente Umsetzung von CO2 ermöglichen.
Damit legt Schuller den Grundstein für eine künftige biotechnologische Produktion von Kohlenstoffverbindungen aus atmosphärischem CO2. Eine vielversprechende biologische Lösung, um den hohen CO2-Gehalt in der Atmosphäre zu verringern, ist das Recycling von Kohlenstoff mit Hilfe acetogener Bakterien. Diese Mikroorganismen können CO2 in großen Industrieanlagen fixieren – und daraus Bio-Kraftstoffe und recycelte Kohlenstoffverbindungen produzieren. Ihr Stoffwechsel ist jedoch noch ein großes Rätsel, an dessen Erforschung Schuller arbeitet.
Wie acetogene Bakterien ohne Sauerstoff atmen können
Die verschiedenen – nicht unbedingt miteinander verwandten, aber immer ohne Sauerstoff lebenden – acetogenen Bakterien nutzen einen speziellen Stoffwechselweg. Sie stellen Acetat (Essigsäure-Salz) her, das sie zur Atmung verwenden, wie andere Lebewesen Sauerstoff. Vermutlich ist dies der älteste biochemische Stoffwechselweg auf der Erde: Aus CO2 und Wasserstoff, die bereits auf der frühen Erde vorhanden waren, bilden die Bakterien organische Verbindungen, also „lebende Materie“.
Schullers Gruppe hat begonnen, die einzelnen enzymatischen Schritte, die dafür notwendig sind, aufzuklären. Dabei charakterisierten sie bislang unbekannte Mechanismen der Enzyme und ihre Rolle im Stoffwechsel der Bakterien. Eins dieser Enzyme kann Wasserstoff direkt zur Reduktion von CO2 nutzen: Diese Wasserstoff-abhängige CO2-Reduktase (HDCR) ist 10.000 Mal effizienter als jeder chemische Katalysator – und damit ein Spitzenkandidat für die biotechnologische Forschung.
„Der Lebensstil solcher Mikroorganismen und ihre Enzyme halten noch viele Geheimnisse bereit“, verspricht Schuller. „Mit unserer Forschung wollen wir zur Lösung gesellschaftlicher Probleme wie dem menschgemachten Klimawandel beitragen, indem wir den Weg für die Nutzung von CO2 als Rohstoff für wertvolle Produkte ebnen“.
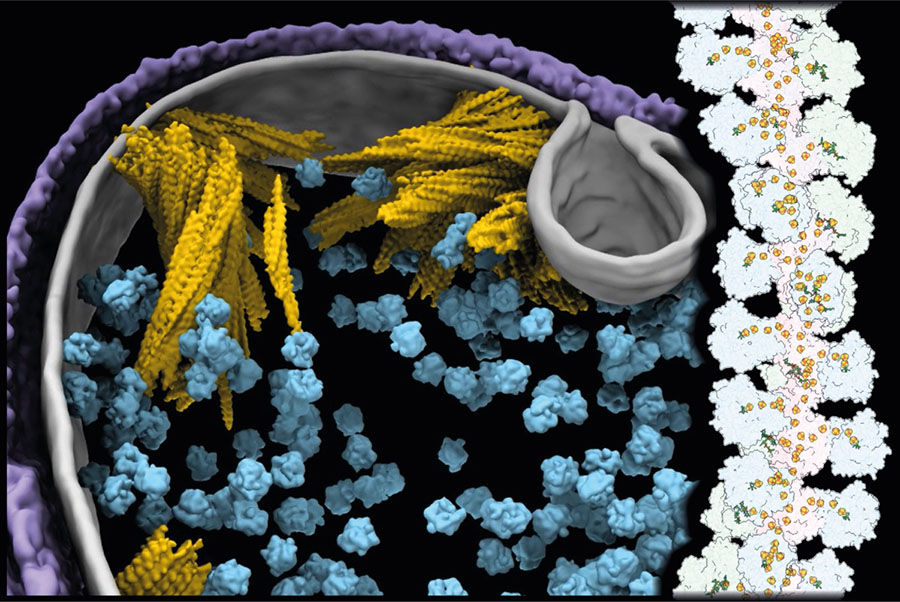
Um die molekulare Grundlage dieses Enzyms zu verstehen untersuchte es Schullers Gruppe mit Hilfe der Kryo-Elektronenmikroskopie. Sie enthüllten eine überraschende Struktur: Das Enzym bildet „Nano-Drähte“, auf denen die enzymatischen Untereinheiten angeordnet sind. Diese ungewöhnliche Architektur erklärt die herausragenden katalytischen Eigenschaften. Je länger der „Draht“ ist, desto höher seine Aktivität. Mutations-Experimente zeigen, dass lange Strukturen die katalytische Aktivität des Enzyms maximieren.
Zelluläre Elektronentomografie lieferte Einblicke in die natürliche Umgebung der Drähte: An der Spitze der Zellen sitzen große ringförmige Strukturen aus verflochtenen „Drähten“. „Wir vermuten, dass diese Organisation eine Anpassung an extreme Umweltbedingungen ist“, erklärt Schuller. Sie gewährleiste eine große Oberfläche mit vielen untereinander verknüpften Reaktionszentren für die Oxidation von Wasserstoff. Damit sind stets ausreichend Elektronen vorhanden, um das in die Zelle diffundierende CO2 einzufangen und zu konzentrieren. Die HDCR ermöglicht also einen acetogenen Kohlenstoff-Konzentrierungsmechanismus, der nötig ist, um unter harschen Bedingungen zu überleben.
Wichtig für diese Studien ist spezielles Handwerkszeug: So gewährleistet ein Schutzgaszelt Sauerstoff-freie Bedingungen für die elektronenmikroskopische Probenvorbereitung. Entsprechend optimierte Mikroben und neuartige synthetische Stoffwechselwege könnten CO2-Emissionen reduzieren und eine nachhaltigere Produktion ermöglichen, die CO2 in den Ressourcenkreislauf einbindet.


